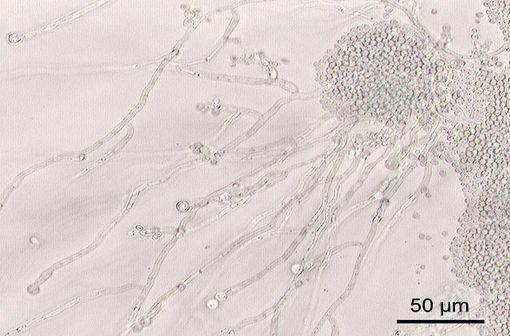
Candida albicans vus au microscope (illustration @Y Tambe sur Wikimedia)
=
= Η ECALTA έλαβε επέκταση της ένδειξης της στην παιδιατρική στις 3 Ιουνίου 2020, στη θεραπεία της επεμβατικής καντιντίαση σε παιδιατρικούς ασθενείς ηλικίας 1 μηνός έως λιγότερο από 18 ετών (|| 326 cf. Encadré 1).
Framed 1 - Θεραπευτική ένδειξη της Ecalta IV (ενδοφλέβια)
Σε αντίθεση με την ένδειξη της εξουσιοδότησης μάρκετινγκ (AMM) στην παιδιατρική, η D'Ecalta δεν περιλαμβάνει ουδετεροπενικούς ασθενείς, όπως στους ενήλικες.
Σημειώστε ότι στα παιδιά, μία δόση φορτίου 3 mg/kg (που δεν υπερβαίνει τα 200 mg) πρέπει να χορηγείται την πρώτη ημέρα, ακολουθούμενη από δόση συντήρησης 1,5 mg/kg (που δεν υπερβαίνει τα 100 mg) την ημέρα τις επόμενες ημέρες.
SMR Σημαντικό σε μη -ουραροπενικούς παιδιατρικούς ασθενείς
Στο γνώμη της 2ης Ιουνίου 2021, η Επιτροπή Διαφάνειας αξιολόγησε την επέκταση της ένδειξης της ECALTA (anidulafungine) σε ασθενείς ηλικίας 1 μηνών έως 18 ετών με βάση τα αποτελέσματα δύο κλινικών μελετών:
Αυτές οι δύο μελέτες έχουν επίσης ενσωματωθεί σε μια φαρμακοκινητική μετα-ανάλυση (PMAR-EQDD-A885BOTHER-865) που φέρνουν επίσης δεδομένα σε ενήλικες (μελέτες A8851011 φάση IV και A8851019 της φάσης IIIB). | Με βάση τα διαθέσιμα δεδομένα σε ενήλικες που έχουν επιδείξει μια διαφορά στην ποσότητα μέτριας επίδρασης της ECALTA σε σύγκριση με την φλουκοναζόλη, ουσιαστικά σε μη -ουροπενικούς ασθενείς με λοιμώξεις σε
Sur la base des données disponibles chez l'adulte ayant démontré une différence de quantité d'effet modeste d'ECALTA par rapport au fluconazole, essentiellement chez des patients non neutropéniques ayant des infections à Candida albicans, και τα διαθέσιμα δεδομένα περιορισμένα σε παιδιά (μελέτη φάσης IIIB), υποδηλώνοντας ένα προφίλ απόδοσης και ανοχής παρόμοια με εκείνη που περιγράφεται σε αυτό που περιγράφεται στον ενήλικα, αλλά με υψηλότερη συχνότητα των ανεπιθύμητων γεγονότων του ήπατος, το CT θεωρεί ότι:
Συμπερασματικά, το CT θεωρεί ότι " σε μη -νευροεπενούς ασθενείς ηλικίας 1 μηνών έως 18 ετών, στην πλειονότητα των περιπτώσεων, η φλουκοναζόλη παραμένει η θεραπεία αναφοράς Στο αντίθετο, σε ουδετεροπενικούς ασθενείς σε ουδετεροπενικούς ενήλικες, η Ecalta δεν έχει χώρο στη θεραπευτική στρατηγική λόγω του χαμηλού επιπέδου αποτελεσματικότητας όσον αφορά τις διαθέσιμες εναλλακτικές λύσεις.
A l'inverse, chez les patients neutropéniques âgés de 1 mois à 18 ans, comme chez l'adulte neutropénique, ECALTA n'a pas de place dans la stratégie thérapeutique en raison du faible niveau de preuve d'efficacité au regard des alternatives disponibles.
για να προχωρήσουμε περαιτέρω
Διάταγμα της 12ης Ιουλίου 2021 Τροποποιώντας τον κατάλογο των φαρμακευτικών ειδικότητες που εγκρίθηκαν για τη χρήση κοινοτήτων και διαφόρων δημόσιων υπηρεσιών - ECALTA | ( ( Επίσημο περιοδικό της 20ης Ιουλίου 2021 - κείμενο 26)
Avis de la Commission de la Transparence - ECALTA (έχει, 2 Ιουνίου 2021)
=
Περίληψη:
Ecalta 100 mg σκόνη για διάλυμα που πρέπει να αραιωθεί για έγχυση ( anidulafungine) επωφελείται από την επέκταση της έγκρισής της σε κοινότητες στην παιδιατρική, σε περιορισμένη ένδειξη σε σύγκριση με την ένδειξη του AM, δηλαδή τη θεραπεία της επεμβατικής καντιδής σε ασθενείς Όχι ουδετεροπενικό ηλικίας 1 μήνα έως <18 ετών.
L' αντιμυκητιασικό νοσοκομείο ECALTA 100 mg σκόνη για αραιό διάλυμα σε έγχυση ( anidulafungine) στην παιδιατρική, στη θεραπεία της επεμβατικής καντιντίαση σε ασθενείςnon ουδετεροπενικό ηλικίας 1 μήνα έως <18 ετών.Ecalta 100 mg σκόνη για διάλυμα που πρέπει να αραιωθεί για έγχυση ( anidulafungine) επωφελείται από την επέκταση της έγκρισής της σε κοινότητες στην παιδιατρική, σε περιορισμένη ένδειξη σε σύγκριση με την ένδειξη του AM, δηλαδή τη θεραπεία της επεμβατικής καντιδής σε ασθενείς Όχι ουδετεροπενικό ηλικίας 1 μήνα έως <18 ετών.
= Η ECALTA έλαβε επέκταση της ένδειξης της στην παιδιατρική στις 3 Ιουνίου 2020, στη θεραπεία της επεμβατικής καντιντίαση σε παιδιατρικούς ασθενείς ηλικίας 1 μηνός έως λιγότερο από 18 ετών (|| 326 cf. Encadré 1).
Framed 1 - Θεραπευτική ένδειξη της Ecalta IV (ενδοφλέβια)
| Θεραπεία διηθητικής καντιντίασης σε ενήλικες ασθενείς και παιδιατρικούς ασθενείς ηλικίας 1 μήνα έως <18 ετών. |
Σε αντίθεση με την ένδειξη της εξουσιοδότησης μάρκετινγκ (AMM) στην παιδιατρική, η D'Ecalta δεν περιλαμβάνει ουδετεροπενικούς ασθενείς, όπως στους ενήλικες.
Σημειώστε ότι στα παιδιά, μία δόση φορτίου 3 mg/kg (που δεν υπερβαίνει τα 200 mg) πρέπει να χορηγείται την πρώτη ημέρα, ακολουθούμενη από δόση συντήρησης 1,5 mg/kg (που δεν υπερβαίνει τα 100 mg) την ημέρα τις επόμενες ημέρες.
SMR Σημαντικό σε μη -ουραροπενικούς παιδιατρικούς ασθενείς
Στο γνώμη της 2ης Ιουνίου 2021, η Επιτροπή Διαφάνειας αξιολόγησε την επέκταση της ένδειξης της ECALTA (anidulafungine) σε ασθενείς ηλικίας 1 μηνών έως 18 ετών με βάση τα αποτελέσματα δύο κλινικών μελετών:
- Μελέτη της μη -συγκριτικής φάσης IIIB (A8851008) μη -συγκρίσεως, ηλικίας από 1 μήνα έως κάτω των 18 ετών: ο κύριος στόχος ήταν να εκτιμηθεί η ασφάλεια και η ανοχή της ανιδούλα και ο ορισμός φαρμακοκινητικών.
- Μια μελέτη φάσης Ι (Duke IIR), μονοκεντρική, που πραγματοποιήθηκε σε 15 παιδιά και νεογέννητα κάτω των 24 μηνών που κινδυνεύουν από τον καντιδισμό και την επεμβατική καντιντίαση: ο κύριος στόχος ήταν ο κύριος στόχος της φαρμακοκινητικής που ειδικά για παιδιά ηλικίας κάτω των 2 ετών.
Αυτές οι δύο μελέτες έχουν επίσης ενσωματωθεί σε μια φαρμακοκινητική μετα-ανάλυση (PMAR-EQDD-A885BOTHER-865) που φέρνουν επίσης δεδομένα σε ενήλικες (μελέτες A8851011 φάση IV και A8851019 της φάσης IIIB). | Με βάση τα διαθέσιμα δεδομένα σε ενήλικες που έχουν επιδείξει μια διαφορά στην ποσότητα μέτριας επίδρασης της ECALTA σε σύγκριση με την φλουκοναζόλη, ουσιαστικά σε μη -ουροπενικούς ασθενείς με λοιμώξεις σε
Sur la base des données disponibles chez l'adulte ayant démontré une différence de quantité d'effet modeste d'ECALTA par rapport au fluconazole, essentiellement chez des patients non neutropéniques ayant des infections à Candida albicans, και τα διαθέσιμα δεδομένα περιορισμένα σε παιδιά (μελέτη φάσης IIIB), υποδηλώνοντας ένα προφίλ απόδοσης και ανοχής παρόμοια με εκείνη που περιγράφεται σε αυτό που περιγράφεται στον ενήλικα, αλλά με υψηλότερη συχνότητα των ανεπιθύμητων γεγονότων του ήπατος, το CT θεωρεί ότι:
- Σε μη -ουραροπενικούς παιδιατρικούς ασθενείς: το s= Η ERVICE Medical Rendered (SMR) της ECALTA είναι σημαντική.
- Σε ουδετεροπενικούς παιδιατρικούς ασθενείς: Το SMR της ECALTA είναι Ανεπαρκής.
Συμπερασματικά, το CT θεωρεί ότι " σε μη -νευροεπενούς ασθενείς ηλικίας 1 μηνών έως 18 ετών, στην πλειονότητα των περιπτώσεων, η φλουκοναζόλη παραμένει η θεραπεία αναφοράς Στο αντίθετο, σε ουδετεροπενικούς ασθενείς σε ουδετεροπενικούς ενήλικες, η Ecalta δεν έχει χώρο στη θεραπευτική στρατηγική λόγω του χαμηλού επιπέδου αποτελεσματικότητας όσον αφορά τις διαθέσιμες εναλλακτικές λύσεις.
A l'inverse, chez les patients neutropéniques âgés de 1 mois à 18 ans, comme chez l'adulte neutropénique, ECALTA n'a pas de place dans la stratégie thérapeutique en raison du faible niveau de preuve d'efficacité au regard des alternatives disponibles.
για να προχωρήσουμε περαιτέρω
Διάταγμα της 12ης Ιουλίου 2021 Τροποποιώντας τον κατάλογο των φαρμακευτικών ειδικότητες που εγκρίθηκαν για τη χρήση κοινοτήτων και διαφόρων δημόσιων υπηρεσιών - ECALTA | ( ( Επίσημο περιοδικό της 20ης Ιουλίου 2021 - κείμενο 26)
Avis de la Commission de la Transparence - ECALTA (έχει, 2 Ιουνίου 2021)
=
για να προχωρήσουμε περαιτέρω
Συμβουλευτείτε τις μονογραφίες Vidal
Πηγές
για να λάβετε όλα τα νέα δωρεάν μέσω ηλεκτρονικού ταχυδρομείου Εγγραφώ!

 3 λεπτά
3 λεπτά Προσθέστε ένα σχόλιο
Προσθέστε ένα σχόλιο

Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.